Complicaciones en el seno maxilar
Autor: Dr. Rodrigo Felipe Naranjo Restrepo
Publicado en: CIB – Corporación para investigaciones biológicas
Editorial: Editora Fondo Editorial – Bogotá – Colombia
Introducción
Diversas son las complicaciones quirúrgicas que se pueden presentar durante la elevación del Piso del Seno Maxilar (EPSM), las más frecuentes son reportadas en la literatura como: perforación de la mucosa de membrana de Schneider, siendo ésta la causa más común debido a la interposición de tabiques óseos dentro del seno maxilar, la presentación de hemorragias, infecciones, desplazamiento de cuerpos extraños dentro de la cavidad, obstrucción del ostium y sinusitis crónica.
A continuación en este capítulo, se revisarán cada una de las complicaciones, su etiología, el tratamiento más frecuente y recomendado en la literatura luego de realizar los procedimientos quirúrgicos que involucran la EPSM.
La literatura clasifica las complicaciones como intraoperatorias, tempranas y tardías. [1]
1) Complicaciones intraoperatorias:
- Perforación de la membrana.
- Fractura del reborde proceso residual.
- Hemorragia.
- Obstrucción del ostium maxilar.
- Daño de dentición adyacente.
2) Complicaciones tempranas:
- Dehiscencia de la herida.
- Infección aguda: sinusitis.
- Exposición de la membrana.
3) Complicaciones tardías:
- Sinusitis crónica.
- Desplazamiento del implante al interior del seno maxilar.
- Mareo o vértigo.
Los factores que pueden aumentar el riesgo al realizar esta técnica son bien descritos por Testori et al,[2] como la edad del paciente y su estado de salud, el hábito de fumar (número de cigarrillos por día), la microgeometría del implante (tamaño, diámetro, forma, longitud), nivel de altura del reborde residual, espesor y calidad de hueso remanente en la zona del proceso alveolar, tipo de material a injertar, tiempo en la colocación del implante inmediato o diferido después de realizar la EPSM.
Es de anotar como factor primordial en la repercusión de la morbilidad con esta técnica que, la indicación en pacientes fumadores de más de 15 cigarrillos por día y con rebordes alveolares menores de 4 mm se debería reconsiderar una y otra vez, antes de realizarla en estos pacientes por el alto riesgo de las complicaciones conexas.
Es importante que el profesional tenga definitivamente un pleno conocimiento de los principios quirúrgicos y de las estructuras anatómicas involucradas en la intervención, su origen embriológico, así como, de la fisiología del seno maxilar, antes de proceder a realizar dicho procedimiento. Asimismo, deberá conocer las diferentes técnicas que se han propuesto para la EPSM e identificar cuáles, son las más utilizadas hoy en día.
EMBRIOLOGÍA DEL SENO MAXILAR
De los senos paranasales, el seno maxilar es el primero en desarrollarse al comenzar la etapa del tercer mes de vida intrauterina. La cavidad del seno maxilar es una invaginación de epitelio nasal del infundíbulo, este estado de desarrollo es llamado proceso de neumatización primaria, que continúa hasta el cuarto mes de vida intrauterina. Durante este proceso, el desarrollo del seno maxilar permanece dentro de la capsula en el infundíbulo etmoidal. [3]
En el quinto mes comienza la segunda etapa de desarrollo del seno maxilar y es llamada neumatización secundaria, esto sucede cuando el primordio del seno maxilar inicia su crecimiento dentro del hueso maxilar. Al nacimiento el seno maxilar tiene dimensiones de 7 mm de longitud anteroposterior, 4 mm de altura y 4 mm de amplitud, su volumen total de 6 a 8 mm. [3]
La cara comienza un desarrollo diferente al del cráneo, donde el seno maxilar se está desarrollando en la cara a una tasa de 2 a 3 mm en sentido antero posterior y se podrá observar radiográficamente a los 5 meses con una forma triangular por debajo del agujero infraorbitario.
El crecimiento posnatal del seno maxilar continúa en sus tres dimensiones con tres picos de desarrollo reconocidos: primero al nacimiento hasta los 2.5 años, segundo de los 7.5 a los 10 años, y el tercero de los 12 a los 14 años.
En esta última etapa termina el crecimiento del seno maxilar con la erupción de los dientes permanentes posteriores, adquiriendo forma piramidal. [4] En este desarrollo final, el piso del seno maxilar se ubica entre 5 a 12 mm por debajo del piso de la fosa nasal, con un volumen de 15 a 12.5cc en total, y presenta unas dimensiones de 38 a 45 mm en sentido anteroposterior, 36 a 45 mm de altura y 25 a 35 mm de amplitud. [5]
No obstante, se presentan dos causas del aumento del tamaño del seno maxilar a través de la vida. La primera es por la pérdida de piezas dentarias posteriores y la subsecuente reabsorción alveolar residual, y la segunda, debido a una presión positiva intrasinusal generada por el tamaño de la apertura antral a la vía nasotraqueal; llevando como consecuencia al crecimiento del volumen del seno maxilar, estos procesos ocurren como resultado de la reabsorción del piso sinusal como consecuencia de un incremento de la actividad osteoclásica perióstica de la membrana de Schneider.
ANATOMÍA DEL SENO MAXILAR
El seno maxilar es una cavidad piramidal, localizada principalmente en el hueso maxilar, pero también se extiende entre los huesos palatinos y malar. La forma de pirámide presenta un ápice extendido dentro del proceso cigomático del maxilar. Se puede distinguir del seno maxilar una base interna (nasal), esta base se encuentra hacia la pared nasal lateral o tabique intersinusal que presenta el meato medio, orificio de comunicación con las fosas nasales; un vértice cigomático o malar (orientado hacia el cuerpo del hueso malar); y tres paredes: una pared superior u orbitaria constituida por una lámina ósea compacta que la separa de la cavidad orbitaria y que tiene como límite el conducto suborbitario que aloja el nervio infraorbitario; una pared posterior, pterigomaxilar o tuberosidad del maxilar, constituida por la parte posterior del maxilar posterior y a su vez está separada por las fosas craneales infratemporal y pterigopalatina; y una pared anteroinferior constituyendo el piso de la pirámide en relación a los ápices dentales.[6]
El seno maxilar varía de forma y de acuerdo a esto se ha clasificado en cuatro grupos: semielipsoidal 15%, parabólico 30%, hiperbólico 47%, y cónicos 8%. Además de acuerdo al volumen interno se pueden identificar 3 tipos de tamaños: grandes 25 cc, medianos 8 a 12 cc y pequeños 2 cc. [7]
El seno maxilar presenta internamente una delgada mucosa de epitelio respiratorio ciliado, siendo su característica principal el peristaltismo en sentido de las manecillas del reloj, generando limpieza mucociliar y llevando todas las secreciones hacia el ostium, el cual está localizado a un nivel más alto que el del piso del seno maxilar. Esta membrana presenta continuidad con el epitelio nasal y es llamada membrana de Schneider, siendo más gruesa que la membrana de otros senos paranasales, pero más delgada y menos vascular que la mucosa nasal. El ostium está situado hacia el lado craneal y conecta el seno maxilar al meato medio de la cavidad nasal. Este se encuentra a 4 cm del piso del seno maxilar, se abre en el hiatus semilunar en el meato medio; en tamaño y forma tiene 2.4 mm en su diámetro y se considera un canal de 3 a 5 mm de longitud.[7]
Es de anotar que el seno maxilar suele estar parcialmente segmentado por la existencia de tabiques incompletos de orientación aproximadamente frontal, que se denominan tabiques intrasinusales. Ocasionalmente (menos del 5% de las veces) llegan a dividir el seno en dos e incluso cinco cavidades distintas. [8,9]
La inervación está regida por el nervio maxilar, da inervación sensorial general, la parte simpática desde el ganglio cervical superior, y parasimpática desde el ganglio esfenopalatino. Estas fibras están distribuidas a través de las ramas del nervio maxilar, como la infraorbitaria y la dental media superior, y a través de las ramas nasales y palatinas mayores del ganglio pterigopalatino. [10]
El hipotálamo da el aporte simpático y parasimpático del seno maxilar. El simpático mediante sinapsis en la columna intermedio-lateral de la médula espinal torácica superior y el ganglio cervical superior, el aporte parasimpático a través de sinapsis en el núcleo salivar superior y el ganglio pterigopalatino. [10]
La irrigación sanguínea es generalmente derivada de dos fuentes vasculares, mucosa y ósea. El suministro sanguíneo de la mucosa proviene de los vasos sanguíneos de la nariz, arteria esfenopalatina externa e interna, las arterias nasales anteriores y posteriores, las cuales entran a través del ostium. La irrigación ósea contribuye al aporte sanguíneo que procede de la arteria maxilar interna a través de la arteria alveolar superior posterior y de la infraorbitaria, además de pequeñas contribuciones de las arterias palatinas y la facial. .[6]
Usualmente se establecen varias anastomosis entre las arterias alveolar posterosuperior a la arteria infraorbitaria que puede ser encontrada dentro y fuera de las paredes óseas que también nutren la membrana de Schneider, como también los tejidos vestibulares epiperiostales. Esta característica permite que los injertos óseos sobrevivan dentro del seno maxilar. [7] Sin embargo, aunque la vascularización de la mucosa sinusal es de tipo anastomótico, hay discrepancia en la literatura por la aparición en unos senos maxilares y en otros no dudando su veracidad. Elian et al[5], encontraron dicha anastomosis en el 53% de los casos, por el contrario, Rosano et al[5], la encontraron en todos los casos. Un año después, los mismos autores detectaron en otro estudio la presencia de un canal óseo bien definido en el 47% de los casos. [5]
El drenaje venoso está a cargo del plexo venoso pterigoideo en su zona posterior, con algunas de las venas faciales en la parte anterior entre sí al convergir hacia el ostium y pasar a través de las fontanelas para unirse a los vasos linfáticos de la membrana mucosa de la pared lateral del meato medio.
FUNCIÓN DEL SENO MAXILAR
Algunos autores afirman que una de sus funciones es humedecer los ojos o la retención de olores antes de transportarlas hacia el cerebro. Actualmente no hay claridad sobre cuál es su principal función. La literatura reporta también las siguientes como funciones. [11,12]
Servir como caja de resonancia en la emisión de sonidos; constituir un sistema mucosilla de limpieza, humidificación y calentamiento del aire inspirado para una efectiva función mucociliar; aligerar la cabeza; constituir cámaras de reserva neumática de las fosas nasales, y ayudar al olfato.
La membrana de Schneider tiene una virtud en el proceso de recuperación rápida, esta es capaz de repararse después de una perforación a causa de un trauma, entre 6 a 8 semanas. [4]
Teniendo en cuenta esta recomendación del autor, no se debería tratar de realizar nuevos procedimientos quirúrgicos para la elevación de la membrana del piso del seno sinusal antes de dos meses, para permitir una adecuada recuperación y estar seguros de que sus funciones relacionadas con la limpieza mucociliar se pueda realizar completamente, así se evitarán complicaciones como infecciones en el seno maxilar.
TÉCNICAS PARA LA ELEVACIÓN DE PISO DEL SENO MAXILAR
Como complemento de la implantología y debido a la limitación de las condiciones anatómicas generadas por la atrofia de los maxilares y la neumatización del seno maxilar, en los años ochenta comienza por parte de diferentes cirujanos la propuesta de una técnica quirúrgica para aumentar en sentido vertical y horizontal la altura del reborde alveolar residual posterior del maxilar superior.
Aunque el primer reporte sobre la colocación de un injerto en el seno maxilar lo realiza Hilt Tatum Jr. (Universidad de San Petersburgo) como alternativa al cubrimiento de una comunicación orosinusal en el Congreso de Alabama de 1976, en 1982 Phillip Boyne y Robert James (Universidad de Lomalinda, California) fueron los primeros en definir la elevación del piso de seno como un “incremento en grosor de la estructura ósea del piso del antrum maxilar a la cresta del reborde alveolar maxilar”. [13] En el consenso de oseointegración en el 2009, se reconoce este procedimiento como parte integral de la implantología y se da la siguiente definición: “un procedimiento de aumento para la colocación de implantes en el maxilar posterior donde la neumatización del seno maxilar o la pérdida vertical de hueso ocurre”. [5,14]
Elevación de piso del seno maxilar
En la actualidad estas técnicas tiene más de 25 años, no hay un consenso definido sobre la cantidad de hueso mínimo residual existente en el reborde alveolar para realizar la EPSM. Varias revisiones sistemáticas reportan que si la altura del reborde alveolar residual es de 3 a 8 mm, la elevación de seno maxilar, dependiendo de la técnica utilizada, puede llevar a menores complicaciones posquirúrgicas y puede dar resultados más predecibles a la hora de conformar un entorno adecuado para colocación de implantes de más de 10 mm.[15]
Actualmente estas técnicas puede ser efectuadas en uno o en dos pasos, dependiendo del tipo de material o la técnica que se va a realizar, además de la cantidad de hueso residual disponible y la posibilidad de poder brindar al implante estabilidad primaria.
Para poder entender las complicaciones que se podrían presentar en la EPSM es indispensable conocer los procedimientos propuestos en la literatura:
Ventana lateral (Caldwell-Luc). La técnica de elevación de seno maxilar, Ventana lateral fue primero descrita en 1893 por George Caldwell (Estados Unidos) y un año más tarde por Guy Luc en Francia.[16] Esta técnica consiste en el abordaje del seno maxilar por vía vestibular a través de la fosa canina, realizando un colgajo vestibular que puede efectuarse a través del surco intrasurcular de las piezas dentales desde el primer molar hasta la zona mesial del canino con una relajante de descarga del colgajo para quedar de frente a la cara quirúrgica del seno maxilar; otra forma descrita de este abordaje es una incisión en el fondo del surco que compromete área de la región vestibular en una forma de colgajo semilunar (imagen) 17-1). Los parámetros establecidos para la técnica se consideraron como una distancia menor de 10 mm entre la cresta del reborde residual y el piso de seno y como mínimo una altura de hueso remanente de 5 o 6 mm.
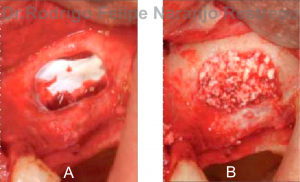
Imagen 17-1. A- Elevación de seno maxilar Ventana lateral (Caldwell-Luc), a la que denominó “elevación de piso de seno maxilar abordaje lateral”. B- Colocación de injerto óseo particulado para llenar el defecto creado. Tomado de Ucer C. Nasal suction technique for maxillary sinus floor elevation: a report of 24 consecutive patients. Int J Oral Maxillofac Implants. 2009; 24(6): 1138-43
Con el advenimiento de nuevas técnicas se empieza a practicar la cirugía endoscópica funcional sinusal (CEFS), siendo ésta la técnica de elección por los otorrinolaringólogos en la actualidad por ser menos invasiva.
Ventana lateral (Tatum). Tatum en la reunión de Alabama en 1976 y posteriormente presentada con algunas modificaciones por Boyne en 1980,[17] quien propone una modificación a la técnica de elevación de seno maxilar Ventana lateral (Caldwell-Luc), a la que denominó “elevación de piso de seno maxilar abordaje lateral”, para esto fracturaba parcialmente la tabla vestibular hacia el interior del seno maxilar con el fin de elevar la membrana sinusal, para luego colocar un injerto autólogo y después a los seis meses, colocar el implante endo-óseo.
Abordaje transcrestal (Summers). La utilización del abordaje crestal para EPSM lo realizó Robert Summers en 1994(18-19-20] , es conocida como técnica transcrestal, se caracteriza por un abordaje del seno maxilar desde la cresta del reborde alveolar en sentido corono-apical, sin necesidad de realizar exposición de las paredes laterales del seno maxilar; se realiza con tres instrumentos llamados cinceles romos, los cuales son instrumentos cónicos graduados en longitud y grosor que se denominan osteótomos, estos instrumentos son formadores de canales que ingresan desde el reborde de la cresta alveolar para establecer la profundidad y dirección del nuevo alvéolo formado, estos expanden lateralmente el hueso vestibular y palatino, y lo compactan conforme se vaya realizando la penetración, se basa en unos parámetros preestablecidos como una distancia menor de 10 mm entre la cresta del maxilar y el piso de seno, como mínimo una altura de hueso remanente de 5 o 6 mm.
A su vez, Summers propone otra técnica, la utilización de osteótomos más adición de hueso. Esta técnica empuja progresivamente el hueso remanente hacia arriba, al tiempo que van elevándose el seno maxilar, el periostio y la membrana, gracias a la masa ósea que se desliza (imagen 17-2). (17-19-20-21]
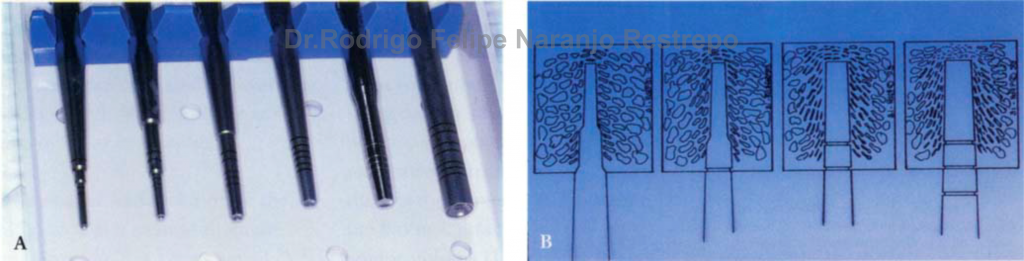
Imagen 17-2. A- Osteótomos propuestos por Summers de diferentes diámetros y B- Esquema que ilustra la técnica para la elevación del seno maxilar a través del reborde alveolar residual permitiendo elevar el seno maxilar, el periostio y la membrana. Summers RB. The osteotome technique: Part 2.The ridge expansion osteotomy (REO) procedure. Compendium. 1994; 15(4): 422, 424, 426, passim; quiz 436
Recientemente Ucer C(21) ha descrito el uso de una técnica de aspiración nasal, para mejora de la facilidad de levantar el revestimiento sinusal mientras se reduce el riesgo de perforaciones El autor describe en la técnica, colocar anestesia local con sedación consciente (propofol y remifentanilo), profilaxis con antibióticos (amoxicilina 1.2 g por vía intravenosa, o claritromicina 500 mg).
Con un colgajo mucoperióstico completo se expone la pared lateral del seno maxilar, utilizando una fresa redonda o un dispositivo piezoeléctrico se levanta la ventana antral, ésta quedará de 10 mm de altura y de 10 a 15 mm de longitud, según lo determinado por la longitud del tramo edéntulo. Se realiza aspiración nasal con una punta de succión Yankauer o una cánula nasofaríngea (n.° 6) insertada en la fosa nasal ipsilateral
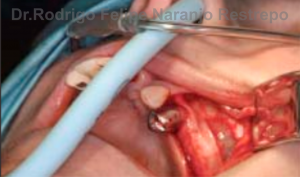
(imagen 17-3) Tomado de: Ucer C. Nasal suction technique for maxillary sinus floor elevation: a report of 24 consecutive patients. Int J Oral Maxillofac Implants. 2009; 24(6): 1138-43.
La succión se aumenta hasta que el efecto de la presión de aire negativa dentro del seno se manifestó por inversión y hacia adentro desplazamiento del revestimiento sinusal. Posteriormente se utilizó colágeno reabsorbible para cubrir interiormente el seno elevado, se coloca el material de relleno óseo. La ventana de acceso lateral se cerró con una membrana de colágeno reabsorbible. [22-23-24]
Cosci y Luccioli, reportaron en el 2000,[25] una nueva técnica de elevación de piso de seno denominada técnica de Cosci, la cual se realiza en rebordes alveolares de más de cuatro milímetros de amplitd y de altura, con el uso de fresas (lifting drills) diseñadas por el autor. El estuche quirúrgico está compuesto por ocho fresas con el mismo diámetro (3.10 mm), ángulo de corte de 30° y longitudes de incremento sucesivo (5, 6, 7, 8, 9, 10, 11 y 12 mm) para ser utilizadas secuencialmente, lo cual es similar al uso de los osteótomos reportados en la técnica de Summers. Ésta técnica está indicada únicamente para colocación inmediata de implantes.
La prevención de las complicaciones de la cirugía de EPSM requiere una evaluación clínica y radiológica cuidadosa de la anatomía del paciente, la calidad del hueso, así como la utilización de una técnica quirúrgica meticulosa. Diferentes estrategias se han descrito para reducir el riesgo de perforaciones, éstas incluyen la disección cuidadosa del material de revestimiento, la utilizando instrumentos de elevación de seno especialmente desarrollados, cirugía con piezoeléctricos, cirugía mínimamente invasiva con condensación hidráulico, o el uso de un globo inflado introducido en la cavidad del seno a través de la osteotomía. Vitkov et al, [24] demostraron el papel de la presión hidráulica durante la elevación cerrada de la membrana sinusal utilizando presión.
COMPLICACIONES INTRAOPERATORIAS
Perforación de membrana
Durante la cirugía de EPSN la complicación quirúrgica más frecuente es la rotura de la membrana de Schneider, [26] ésta complicación está relacionada con la presencia de tabiques óseos localizados dentro de la luz del seno. Para poder confirmar y encontrar las posiciones de estos tabiques óseos, la tomografía ósea tridimensional es la mejor ayuda, como se confirma en el estudio realizado por Neugebauer et al. [8]
La prevalencia de tabiques óseos reportada con radiografía panorámica es de 13 y 14%, mientras que, con estudios de tomografía la presencia de tabiques muestra una prevalencia de 47%. Clínicamente se reportan en 57.6% de los casos, de los cuales el 20.3% están en la zona anterior relacionados con premolares y caninos, y el 25%en la zona posterior en el área de molares.
La perforación de la membrana se realiza principalmente en relación al segundo molar por causa de su raíz palatina, siendo más común en mujeres entre 45 y 59 años. Asimismo, se debe considerar que el seno maxilar suele estar parcialmente compartimentado por la existencia de tabiques incompletos con orientación frontal, que se denominan tabiques medio o central. [27]

(imagen 17-4) Tomado de articulo Neugebauer J, Ritter L, Mischkowski RA, Dreiseidler T, Scherer P, Ketterle M, et al. Evaluation of maxillary sinus anatomy by cone-beam CT prior to sinus floor elevation. Int J Oral Maxillofac Implants. 2010; 25(2): 258-65.
A continuación en la tabla 17-1 se pueden observar varios estudios que muestran la presencia de tabiques en los senos maxilares.
Tabla 17.1. Estudios en humanos que reportan prevalencia del tabique en el seno maxilar, organizados por año de publicación. Tomada de: Briceño JF, Estrada JH. Elevación de piso de seno maxilar: consideraciones anatómicas y clínicas. Revisión de la literatura. Univ Odontol. 2012; 31(67): 27-55.
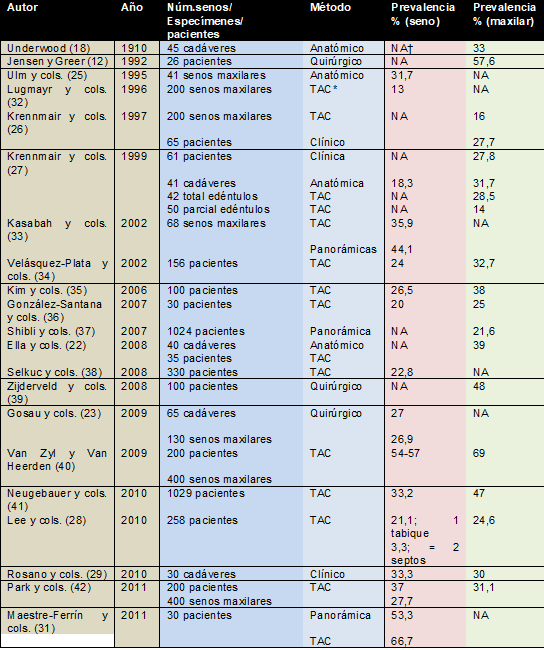
* TAC: tomografía axial computarizada; † NA: no aplica
El uso intraoperatorio de sinuscopia en 1990 para la elevación de seno maxilar, permite eliminar obstáculos como patologías o tabiques óseos y mejora el control sobre la posición del injerto óseo, facilitando un menor riesgo de perforaciones de la membrana sinusal y menos complicaciones postoperatorias en un 39.40%. Ésta técnica permite ver en tiempo real por el operador, la capacidad de deformación de la membrana de Schneider durante la instrumentación, la adición progresiva del injerto óseo, y la colocación del implante. Además logro confirmar que no hay diferencias estadísticamente significativas en las tasas de perforación de la membrana sinusal del seno maxilar entre los métodos quirúrgicos como la técnica modificada de Summers y la técnica de presión mecánica e hidráulica. [28]
En la literatura existe la clasificación para este tipo de perforaciones, la cual está relacionada con el lugar donde se encuentra y el tamaño. Vlassis et al, [29] ilustra 5 tipos de perforaciones existentes cuando se realiza la técnica de elevación de la mucosa sinusal y confirmado que la Clase I y Clase II perforaciones son más fáciles de reparar, mientras que la clase IV es el más difícil de tratar con éxito .
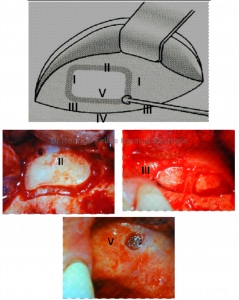
Imagen 17-4. Vlassis et al, [29] ilustra 5 tipos de perforaciones existentes cuando se realiza la técnica de elevación de la mucosa sinusal y confirmado que la Clase I y Clase II perforaciones son más fáciles de reparar, mientras que la clase IV es el más difícil de tratar con éxito
Tratamiento de perforaciones. La perforación de la membrana sinusal como ya se ha discutido es la complicación más frecuente, pero poco se ha hablado acerca de su manejo. La interposición de membranas como opción terapéutica para cubrir dichas perforaciones puede ser una de las alternativas de manejo. Oh y Kraut, no observaron diferencias entre el grupo perforado y el no perforado (99% y 97%, respectivamente). [30]
También se ha sugerido la sutura de la membrana, Robiony et al, [31] recomiendan una técnica simple y fácil de realizar, utilizando una sutura Vicryl 4/0 y posteriormente colocando una membrana de colágeno. A su vez, Hernández et a l[32] realizaron el seguimiento de 104 perforaciones de membrana de Schneider y encontraron que las diferencias no eran significativas estadísticamente entre el porcentaje de supervivencia del implante en sitios perforados en relación con su extensión.
Dicho estudio corrobora los resultados descritos por Vlassis y Fugazzotto, [29] quienes dan importancia a la influencia de la extensión de la perforación en el resultado a largo plazo. Fugazzotto propuso una clasificación de las perforaciones en 3 tipos: 1. Clase I, bordes apicales de la ventana, 2. Clase II, bordes laterales y crestales, que a su vez se pueden subdividir en mesial, distal o crestal dependiendo de su posición en relación con su extensión al seno maxilar subyacente, y 3. Clase III, cualquier ubicación dentro del cuerpo de la ventana preparada. La perforación tipo II también se subdivide en dos clases que son distintas de abordar terapéuticamente: la perforación Clase IIA, donde la osteotomía se extiende 4-5 mm más allá́ de la perforación, bien sea lateral o coronal; y la perforación Clase IIB, que se observa cuando la perforación se encuentra a la altura del borde de la cavidad del seno.
Wallace [33] sugiere una serie de recomendaciones generales para prevenir dichas perforaciones cuando se realiza el procedimiento de EPSM.
- Realizar un diagnóstico prequirúrgico con tomografía axial computarizada (TAC).
- Lograr que la ventana quede en una ubicación determinada (a tres milímetros del piso y la pared anterior).
- Elevar la membrana de lateral a medial, manteniendo el instrumento sobre el hueso en todo momento.
- Todas las reparaciones deben ser estables.
- Las perforaciones muy pequeñas pueden autorrepararse por un pliegue de la membrana o por la formación del coagulo y no requieren membranas.
- A grandes perforaciones, grandes reparaciones que sobrepasen la perforación para brindar estabilidad, se deben fijar para evitar que se desplace el injerto.
- Las reparaciones grandes tienden a desplazarse apicalmente cuando se colocan los injertos.
- Las membranas de reparación se prefieren firmes pero que se puedan deformar.
La perforación inadvertida de la membrana sinusal es una complicación frecuente encontrada durante la elevación del suelo sinusal. Se han desarrollado diferentes estrategias para la prevención o tratamiento de perforaciones, ejemplo de esto es una nueva técnica de aspiración nasal en la que se utilizó la presión de aire negativa antral para facilitar la elevación de la mucosa sinusal y reducir el riesgo de perforaciones que ocurren durante la elevación del suelo sinusal. [22-24]
Fractura del reborde proceso residual
La fractura del reborde residual cuando se realiza la técnica de EPSM es una de las complicaciones tempranas durante el procedimiento y ésta principalmente ocurre cuando la neumatización del seno maxilar es demasiado grande a causa del aumento del tamaño de este a través de la vida. La literatura menciona que la pérdida de piezas posteriores generan pérdida del aporte sanguíneo en el proceso alveolar y se genera la subsecuente reabsorción alveolar residual; también se ha propuesto que la falta de fuerzas oclusales sobre los rebordes conlleva a la disminución progresiva de estos, adicionalmente, se considera que debido a una presión positiva intrasinusal generada por el tamaño de la apertura antral a la vía nasotraqueal lleva como consecuencia a un aumento del volumen del seno maxilar. Este proceso ocurre como resultado de la reabsorción del piso sinusal como consecuencia de un incremento de la actividad osteoclastica perióstica de la membrana de Schneider.
Para evitar dicha complicación es deber del cirujano cuando realiza la técnica quirúrgica, realizar una valoración clínica en la que se realice una palpación y sondaje de la zona para evaluar el grosor de la mucosa. También es necesaria una evaluación radiográfica a fin de observar la morfología del reborde. [34,35]
Por su parte Misch, [36,37] a partir de la sensación táctil del reborde y de su ubicación, realiza una clasificación de densidad ósea únicamente, donde reporta la prevalencia en distintas zonas de los maxilares en 200 pacientes. Tiziano, también en su estudio de análisis de factores de riesgo seguido de aumento de elevación de seno maxilar en un estudio multicéntrico retrospectivo, concluye que rebordes residuales menores de 4 mm aumentan los riesgos y las complicaciones cuando se realiza en pacientes fumadores y el riesgo de infecciones en estos pacientes puede aumentar en 5.6%. [2]
La EPSM ha sido propuesta e investigada durante más de veinte años, no hay un criterio definido sobre la cantidad de hueso mínimo del reborde residual y el piso del seno maxilar para realizar este abordaje. Varias revisiones sistemáticas reportan que si la altura de reborde alveolar residual debe ser minimo de de 3 a 8 mm, la elevación de seno maxilar, dependiendo de la técnica utilizada, puede llevar a menores complicaciones posquirúrgicas y puede dar resultados más predecibles a la hora de conformar un entorno adecuado para colocación de implantes de más de 10 mm. [15]
Hemorragia
La vascularización de la pared anterolateral del seno maxilar se caracteriza por la presencia de anastomosis intraóseas entre la rama dental de la parte posterior de la arteria alveolar superior (AAS), también conocida como la arteria antral alveolar (AAA), y la arteria infraorbitaria (AIO). Tales anastomosis fueron identificadas por la tomografía computarizada en sólo el 53% de los casos. Sin embargo, las anastomosis se encontraron dentro del hueso cortical de la pared lateral del seno maxilar a una distancia variable de la cresta alveolar del maxilar posterior en todos los casos, el sangrado excesivo puede ocurrir durante la preparación de la ventana lateral del seno maxilar en la elevación de la membrana del seno. Aunque la laceración causada de manera accidental no es peligrosa para la vida, puede comprometer el procedimiento. El manejo podría ser la ligadura.[38]
El sangrado intraoperatorio se ha reportado desde el 2% el cual resulta de lacerar o dañar las ramas vasculares de la pared lateral del seno y de los tejidos blandos circundantes. [39] Anavi et al,[40] reportaron un 4,5% de incidencia de sangrado intraoperatorio en 153 pacientes intervenidos.
Wallace sugiere las siguientes recomendaciones cuando se produce el sangrado o para prevenirlo: [33]
- Usar presión directa sobre el punto sangrante.
- Preferiblemente emplear un vasoconstrictor localizado en la zona.
- Usar cera de hueso si es posible.
- Presionar fuertemente el canal de hueso alrededor de los vasos.
- Usar electrocauterio (especial cuidado con la cercanía de la membrana de Schneider).
- Realizar sutura del vaso proximal al punto de sangrado.
La prevención es el mejor tratamiento para cualquier complicación y es por eso que para evitar una laceración de estas anastomosis, se debe tener en cuenta su localización a partir de la efectividad del TAC con cortes trasversales.
Obstrucción del ostium maxilar
Para poder comprender como podría obstruirse el ostium del seno maxilar es necesario regresar un poco a la anatomía y fisiología del seno maxilar, el cual tiene una altura de 36 a 45 mm, la media anchura mesiodistal es de 25 a 35 mm, y la profundidad media es 38 a 45 mm (lateralmente en sentido medial). El volumen del seno maxilar en promedio total es de 13.6 ± 6.4cc. El volumen mínimo del seno maxilar es de 3.5 cc, mientras que el máximo es de 31.8cc.[27]
El seno maxilar presenta internamente una delgada mucosa de epitelio respiratorio ciliado cuya característica es el peristaltismo en sentido de las manecillas del reloj, generando limpieza mucociliar y llevando todas las secreciones hacia el ostium, el cual está localizado a un nivel más alto que el piso del seno maxilar. Esta membrana presenta continuidad con el epitelio nasal siendo más gruesa que la membrana de otros senos paranasales, pero más delgada y menos vascular que la mucosa nasal. El ostium está situado hacia el lado craneal y conecta el seno maxilar al meato medio de la cavidad nasal. Este se encuentra a 4 cm del piso del seno maxilar se abre en el hiatus semilunar en el meato medio, en tamaño y forma tiene 2.4 mm en su diámetro y se considera un canal de 3 a 5mm de longitud. [7]
Esta información se puede utilizar para prevenir las complicaciones del seno maxilar, tales como sinusitis por la obstrucción del ostium cuando se realiza la elevación de la membrana y se pretende sobrepasar estas longitudes anatómicas. Las tomografías lineales permiten evaluar longitudes y posiciones anatómicas del complejo osteo-meatal, las cuales son cruciales para evaluar plenamente la salud fisiológica del seno maxilar y la posibilidad de evitar las infecciones siguientes al injerto óseo maxilar.[41] La obstrucción ostial puede ser causada por la hinchazón posoperatoria de la mucosa maxilar, un hematoma, migración de partículas de injertos óseos que pueden ser llevadas por el peristaltismo de la mucosa de Schneider, a causa de perforaciones al momento de la elevación de esta mucosa, migración del material de regeneración, y seroma. La hinchazón de la mucosa puede conducir a la reducción de la permeabilidad de la unidad osteomeatal, esta unidad tiene un papel clave en el desarrollo de la sinusitis, a través del deterioro del sistema de limpieza mucociliar.
Otra causa de obstrucción de ostium es la falta de asepsia durante la elevación de seno, generando infección dentro del seno maxilar.[42]
Recomendaciones para prevenir la obstrucción del ostium. Las imágenes radiográficas del complejo osteo-meatal son cruciales para evaluar plenamente la salud fisiológica del seno maxilar y la posibilidad de evitar las infecciones siguientes al injerto óseo maxilar.
El mantenimiento de la fisiología del seno maxilar normal debe ser un objetivo de mayor importancia, mientras que la permeabilidad del ostium debe ser preservada. Por lo tanto, el uso de un descongestionante sistémico, tal como pseudoefedrina, y un aerosol nasal que contiene un vasoconstrictor, tal como fenilefrina, oximetazolina se recomienda después de la cirugía de EPSM.[43]
Evitar la perforación de la membrana sinusal. Las perforaciones pequeñas no controladas pueden contribuir al desplazamiento de partículas al ostium; siempre que ocurra esto se deben colocar membranas amplias y suficientes que aíslen el resto de la membrana de Schneider.
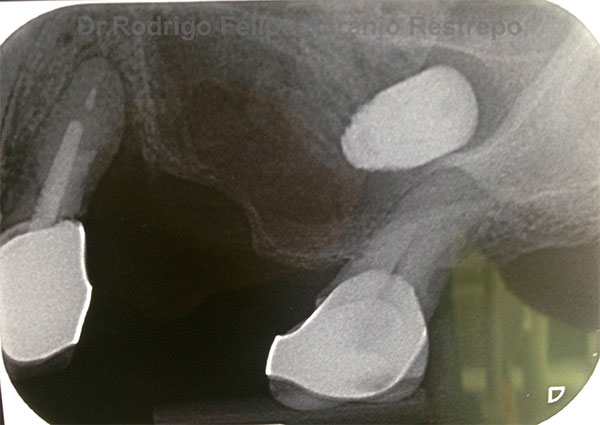
(imagen 17-5) radiografía donde se observa implante desplazado dentro del seno maxilar
Daño en la dentición adyacente
El seno maxilar varía de forma y de acuerdo a esto se ha clasificado en cuatro grupos: semielipsoidal 15%, parabólico 30%, hiperbólico 47% y cónicos 8%. Además de acuerdo al volumen interno se pueden identificar 3 tipos de tamaños: grandes 25 cc, medianos 8 a 12cc y pequeños 2cc. [7] En su porción más anterior, el seno maxilar se extiende generalmente hasta la región comprendida entre el canino y el primer premolar, y en la zona posterior puede comprometer hasta el segundo molar. [17]
El abordaje del seno maxilar por vía vestibular a través de la fosa canina, se realiza con un colgajo vestibular que puede realizarse intraauricular a las piezas dentales desde el primer molar hasta la zona mesial del canino con una relajante de descarga del colgajo para quedar de frente a cara quirúrgica del seno maxilar. Otra alternativa de abordaje, es una incisión en el fondo del surco que involucra la mucosa vestibular mediante un colgajo semilunar; esta técnica, es la que con mayor facilidad puede generar la complicación que aquí se menciona sobre el daño en la raíz del primer molar o del canino, o en su defecto del segundo molar cuando el primero molar está ausente. Es por esto que el operador debe evaluar muy bien con tomografía. [27,44,45 La distancia y la altura de las paredes laterales del seno con relación a las piezas remantes durante la técnica quirúrgica de EPSM y se recomienda además levantar el colgajo amplio, realizar trasiluminación para evaluar con más claridad la posición de las raíces.
Si ocurriera un daño de alguna de las raíces con la fresa durante la osteotomía al realizar la ventana lateral y lesionara los dientes adyacentes podrían ocurrir dos situaciones clínicas, la primera es que el operador se dé cuenta rápidamente de su error y suspenda la acción; en éste caso probablemente no hay compromiso de la vitalidad del diente y sólo se requiere seguimiento para descartar compromiso pulpar. En segundo lugar, al contrario, si el operador no se da cuenta de su error y compromete la pulpa de la pieza dentaria vecina, es indispensable realizar remisión al endodoncista para que defina la necesidad o no de tratamiento de endodoncia.
COMPLICACIONES TEMPRANAS
Dehiscencia de la herida
La complicación posoperatoria temprana más común es la dehiscencia, la cual ocurre a veces en los primeros 10 días.[46] Los factores que contribuyen a la de dehiscencia son la tensión del colgajo, enfermedades nutricionales y sistémicas como diabetes, pacientes consumidores de drogas como alendronatos, fumadores crónicos, trauma mecánico continuo o la irritación con los materiales adicionales que se colocan durante el procedimiento como injertos óseos, membranas de teflón o de colágeno; también el aflojamiento del tornillo de la cubierta, las incisiones incorrectas y la contaminación del injerto óseo, pueden llevar a la formación de secuestro de restos de hueso que podrían ser causa de las dehiscencias,[47] llevando a una eventual pérdida temprana del procedimiento.
Para evitar la dehiscencia de la herida, el cierre sin tensión debe realizarse utilizando unas incisiones de descarga bucal, las dentaduras deben ser aliviadas con un acondicionador de tejidos y se deben realizar suturas de colchonero combinadas con suturas interrumpidas las cuales también son útiles. Cuando la dehiscencia es pequeña y se produce dentro de 24 a 48 horas, el cirujano puede re-suturar la dehiscencia. Una vez que el diámetro de la herida es grande (de 2 a 3 cm) o el tiempo transcurrido es mayor a 2 días, se sugiere que los márgenes de la herida se aviven. [46,48] Si la sutura no es posible, otra alternativa a considerar es el uso de enjuagues de clorhexidina dos veces al día o la prescripción de antibióticos sistémicos deben ser considerados.
Infección aguda: sinusitis
Se podría definir la palabra sinusitis a partir de “sinus” (cueva o cavidad) e “itis” inflamación. “La sinusitis se define como la inflamación de la mucosa o del hueso subyacente de las paredes de uno o más senos paranasales que generalmente obedece a una infección por agentes bacterianos, virales u hongos, lo cual hace que se acumulen secreciones en su interior”. [49]
La prevalencia de infección postoperatoria es relativamente baja. Barone et al[50] reportaron una prevalencia del 5.6%, mientras Pjetursson et al, informaron de una frecuencia del 2.9% (0-12%). [51]
Dolor, inflamación, fistulas, secreción purulenta, dehiscencia del colgajo y supuración son signos de sinusitis, además el aumento de la presión intrasinusal puede ser un factor secundario que puede resultar en bloqueo del drenaje sinusal. Se propone teóricamente que las causas por las cuales aparece sinusitis después del procedimiento de aumento en el piso de seno maxilar son, perforación de la membrana de Schneider, obliteración posoperativa del ostium, producción deficiente de mucus y función ciliar deficiente.
Cronológicamente para que la sinusitis se instaure después de un procedimiento de EPSM es indispensable que ocurra un ciclo: 1. bloqueo del ostium, 2. cogestión de la mucosa, 3. retención de secreciones, 4. espesamiento de las secreciones y alteración del o intercambio gaseoso, 5. daño de los cilios de la mucosa, 6. contribución de un medio de cultivo, 7. retención de secreciones, 8. inflamación e infección bacteriana.[52]
La sinusitis se clasifica en cinco categorías [53] a) sinusitis maxilar, que puede durar hasta cuatro semanas y puede dividirse sintomáticamente en severa y no severa; b) sinusitis aguda recurrente, cuando cuatro o más episodios de sinusitis aguda ocurren dentro de un año; c) sinusitis subaguda, cuando una infección dura de cuatro a doce semanas, como una transición entre sinusitis aguda y crónica; d) sinusitis crónica, cuando los signos y síntomas duran por más de doce semanas, y e) sinusitis crónica de exacerbación aguda, cuando los signos y síntomas de la sinusitis crónica se exacerban, pero retornan a su línea de base después de ser tratada la sinusitis.
La Organisacion Mundial de la Salud OMS clasifica la sinusitis por su duración, puede ser aguda con menos de 4 semanas, subaguda con 4 a 12 semanas y crónica aquella con más de 12 semanas. [54]
Las sinusitis pueden ser de acuerdo a su etiología, infecciosa con predominio de bacterias aerobias (Streptococcus neumoniae, Haemophilus o Moxarella catarralis), alérgica o mixta y viral con predominio de virus como (Rhinovirus spp., Adenovirus spp., Influenza spp. y Parainfluenza spp.).[53] En general, en la fase temprana la secreción nasal con tos persiste por diez días o más. En la sinusitis bacteriana se observa además de lo anterior, fiebre y secreción nasal purulenta con goteo posnasal persistente, edema de la membrana nasal y malestar.
La utima actualizacionn de [55] se hicieron recomendaciones importantes acerca de que se debe distinguir entre rinosinositis bacterianana aguda (RSBA) y rinosinusitis aguda (ARS) causada por infecciones respiratorias virales y condiciones no infecciosas y se debe confirmar un diagnóstico clínico de la rinosinositis crónica (CRS) con la documentación objetiva mediante rinoscopia anterior y endoscopia nasal. Las recomendaciones de manejo deben ser:
1) O bien se debe esperar vigilante (sin antibióticos) o prescribir el tratamiento antibiótico inicial para adultos con RSBA sin complicaciones.
2) Se debe prescribir amoxicilina con o sin clavulin como terapia de primera línea para 5 a 10 días (si se toma la decisión de tratar RSBA con un antibiótico)
3) Se debe reevaluar al paciente para confirmar RSBA, se debe pensar en otras causas de la enfermedad y detectar complicaciones si el paciente empeora o no mejora con la opción de manejo inicial por 7 días después del diagnóstico.
4) Se debe distinguir CRS y ARS si se presentan recurrentes, de episodios aislados de RSBA y otras causas de los síntomas nasosinusales.
5) Se debe evaluar al paciente con posible CRS o ARS recurrentes y se debe entonces sospechar en enfermedades crónicas que pueden perpetuar el problema, como el asma, la fibrosis quística, estado inmunodeprimido, y discinesia ciliar.
6) Se debe confirmar la presencia o ausencia de pólipos nasales en un paciente con CRS.
7) se debe recomendar la irrigación salina nasal, los corticosteroides intranasales tópicos, o ambos para aliviar los síntomas de CRS.
También se recomienda: 1) analgésicos, esteroides intranasales tópicos o irrigación salina nasal para el alivio sintomático de la rinosinusitis viral; 2) Analgésicos, esteroides intranasales tópicos o irrigación salina nasal para el alivio sintomático de RSBA; 3) Obtener pruebas para la alergia y la función inmune en la evaluación de un paciente con CRS o ARS recurrentes; 4) No se deben obtener imágenes radiográficas de los pacientes que cumplen los criterios diagnósticos de ARS, y 5) no se debe prescribir la terapia antifúngica tópica o sistémica en pacientes con CRS.
La sinusitis aguda suele manifestarse a los 10 días después del procedimiento cronológicamente, aunque el paciente días después de la cirugía comienza con sintomatología que puede manifestarse desde un principio como rinitis aguda, presencia de rinorrea purulenta, obstrucción nasal, dolor facial, así́ como fiebre, tos, fatiga, hiposmia o anosmia, dolor dental maxilar y plenitud ótica. En una tomografía se podría observar una mucosa hipertrofiada. [56]
Como tratamiento de la sinusitis aguda se sugiere realizar antibioticoterapia durante ocho días dependiendo del germen causal (Tabla 17-2 y 17-3).
Antibióticos de primera elección: 10 a 14 días.[54]
- Amoxicilina 500 mg c/8 h.
- Trimetoprima /sulfametoxazol
160/800mg c/12 h.
En caso de alergia o intolerancia a los antibióticos de primera elección por 10 a 14 días.
- Doxiciclina100 mg c/12 h.
- Azitromicina 500 mg por 3 días.
- Claritromicina 500 mg c/12 h.
- Cefalosporinas o quinolonas.
La alternativa para casos resistentes o de hipersensibilidad son:
- Clindamicina.
- Rifampicina.
- Quinolonas.
- Cefalosporinas.
Niveles intermedios de resistencia o susceptibilidad reducida a la amoxicilina son susceptibles a un duplicado 34 g/día para los adultos, en dosis fraccionadas. La prescripción simultánea de antiinflamatorios, bien sea esteroideos o no esteroideos, reduce la duración de los síntomas y la intensidad de los dolores. El uso de descongestionantes tópicos como la oximetazolina al 0.5% 3 a 4 veces al día por 3 a 4 días.
El tratamiento de rinosinusitis incluye el manejo del dolor. Se recomiendan analgésico de acuerdo a la severidad del dolor.
En aquellos pacientes que presentan fiebre y dolor se recomienda:
- Paracetamol 500 mg c/6 horas por vía oral en caso de fiebre o dolor.
- Naproxeno 250mg c/12 horas por vía oral durante 5 a 7 días.
Los antihistamínicos, descongestionantes, esteroides, la irrigación con solución salina y los mucolíticos no han sido aprobados para uso en la rinosinusitis.
No hay estudios que apoyen el uso de antihistamínicos durante la rinosinusitis aguda, su uso puede empeorar la congestión y la sequedad de la mucosa nasal.[53]
Tabla 17-2. Esquemas recomendados por diferentes organismos.
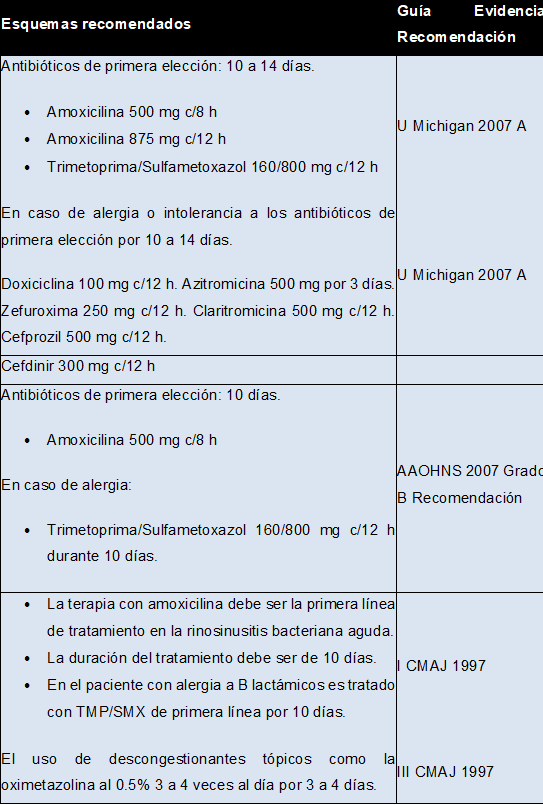
Tomada de: Guía de Práctica Clínica, Diagnóstico y tratamiento de sinusitis aguda, México: Secretaria de Salud; 2009.
Tabla 17-3. Medicamentos indicados en el tratamiento de sinusitis aguda.
Tomada y modificada de: Guía de Práctica Clínica, Diagnóstico y tratamiento de sinusitis aguda, México: Secretaria de Salud; 20
Ahovuo et al,[56] encontraron en su revisión sistemática de ensayos clínicos aleatorizados (ECA) entre 1950 y 2007 (Medline) y 1974 (EMBASE) hasta el 2007 que a la hora de comparar cefalosporinas/macrólidos con amoxicilina-ácido clavulámico, hubo una respuesta estadísticamente significativa en favor de la combinación amoxicilina-ácido clavulámico a los quince días de seguimiento.
En conclusión, encontraron que los antibióticos más utilizados en sinusitis aguda fueron las penicilinas con una efectividad en el 80% de los participantes por dos semanas. Aclaran que su beneficio durante más de dos semanas es mínimo y sugieren otro tipo de tratamiento en caso de no verse mejoría.[57]
Exposición de la membrana
Esta complicación está íntimamente relacionada con la dehiscencia, la cual ocurre a veces en los primeros 10 días.[46]
Los factores que contribuyen a la exposición de la membrana son: la tensión del colgajo demasiado excesiva, enfermedades nutricionales y sistémicas como diabetes, pacientes consumidores de drogas como alendronatos, trauma mecánico continuo en pacientes portadores de placas estéticas o la irritación con los materiales adicionales que se colocan en el procedimiento de elevación de la membrana del piso sinusal como injertos óseos , membranas de teflón o de colágeno demasiado rígidas, también el aflojamiento del tornillo o de las tachuelas que en algunos procedimientos se utilizan para dar estabilidad, la realización de incisiones incorrectas.[47]
Todo lo anterior puede llevar a una eventual pérdida temprana del procedimiento de EPSM. Para evitar la exposición de la membrana en la zona de la de la herida, se debe realizar un cierre sin tensión utilizando unas incisiones de descarga bucal. Las dentaduras o placas estéticas deben ser aliviadas con un acondicionador de tejidos. Se deben realizar suturas de colchonero combinados con suturas interrumpidas, las cuales también son útiles estabilizar adecuadamente las membranas y cuando la dehiscencia es pequeña y se produce dentro de 24 a 48 horas, el cirujano debe volver a suturar la herida y cubrir nuevamente la membrana previa irrigación con clorhexidina si ésta no está infectada y con supuración . Una vez que el diámetro de la herida es grande (de 2 a 3 cm) o el tiempo transcurrido es mayor a 2 días, se sugiere que si hay infección, el retiro de la membrana es lo más adecuado y se debe comenzar terapia antibiótica si el paciente no está en tratamiento.
COMPLICACIONES TARDÍAS
Sinusitis crónica
La rinosinusitis puede ser clasificada por la duración como rinosinusitis aguda (ARS) si la duración es de menos de 4 semanas, o rinosinusitis crónica (CRS) si dura más de 12 semanas, con o sin exacerbaciones agudas. La ARS puede clasificarse además por presunta etiología, con base en los síntomas y la evolución en el tiempo en la rinosinusitis aguda bacteriana (RSBA) o rinosinusitis viral (VRS). Es necesario distinguir entre la etiología bacteriana o infección viral, es importante porque el tratamiento antibiótico es apropiado para el primero. Cuando los pacientes tienen cuatro o más episodios anuales de rinosinusitis, la afección se denomina CRS recurrente. [58]
La sinusitis postoperatoria es la complicación posquirúrgica biológica más frecuentemente reportada por otorrinolaringólogos.[59]
Entre el 3 y el 14% es el porcentaje sinusitis postoperatoria a causa de obstrucción del complejo osteomeatal por procesos inflamatorios como resultado de problemas dentales (endodoncia o periodontal) y alergias relacionadas con cambios inflamatorios. Los quistes de retención en la mucosa (seudoquistes) también pueden afectar el orificio; sin embargo, estas lesiones no parecen responder a antibióticos o medicamentos antinflamatorios y deben ser diagnosticadas con una documentación objetiva, mediante rinoscopia anterior y endoscopia nasal. [55]
En el examen rinoscópico se observa una mucosa congestionada, recubierta de secreciones serosas o purulentas y síntomas que persisten por más de doce semanas.[60-61]
Brook reporta la presencia de pequeñas cantidades de Fusobacterium nucleatum y Prevotella intermedia de infecciones dentales y periodontales,[53] y sugieren una relación entre engrosamiento de la membrana de Schneider y la periodontitis severa. Falk et al, [62] observaron en pacientes con bolsas periodontales mayores a 4 mm en dientes premolares y molares superiores que el engrosamiento de la membrana de Schneider estaba presente radiográficamente y se encontró una disminución del grosor de la membrana de Schneider en todos los cuadrantes cuando se realizó terapia de mantenimiento periodontal con una normalización completa del grosor en el 16%.
Para evitar complicaciones en sinusitis crónicas con la EPSM es indispensable el diagnóstico previo de la condición del seno maxilar y como protocolo de manejo de las sinusitis crónicas es indispensable confirmar la presencia y ausencia de pólipos, el manejo se debe realizar con irrigación con solución salina e inhaladores con corticoesteroides intranasales y no suministrar terapia antifúngica, se debe realizar un test de alergias y función autoinmune, y si el manejo médico no mejora, la alternativa quirúrgica podría ser una opción de tratamiento.[55] cabe anotar que estos casos se debe remitir el paciente al Otorrinoralingolo ORL Para que diagnostique y trate dicha patologia
Desplazamiento del implante al seno maxilar
Generalmente esta complicación es causada por una pérdida de estabilidad primaria o inicialmente inadecuada del implante. [63] Es frecuente que en la técnica de EPSM se realice colocación simultánea de implantes para aquellos casos que tengan un mínimo de 4 a 5 mm de cresta ósea residual. Peleg et al,[64] reportaron éxito tras la técnica simultánea en 1 a 2 mm de cresta ósea, sin embargo, este procedimiento con este espesor aumenta el riesgo de desplazamiento del implante. En paciente fumadores de más de 15 cigarrillos día y rebordes menores de 4 mm se debería pensar y repensar antes de realizarla por el alto riesgo de complicación. [2]
Diferentes técnicas de imagen pueden ser útiles para la localización del cuerpo extraño dentro del seno maxilar, como un radiografía periapical o una radiografía panorámica, y si se requiere mayor especificidad, una tomografía computarizada en 3 dimensiones (TC) con reconstrucción debería ser la ideal. [64] La cirugía endoscópica se utiliza en el caso del desplazamiento de los implantes en el seno maxilar, en asociación con o sin signos y síntomas de la sinusitis u obstrucción del ostium maxilar. La sedación se utiliza con cirugía endoscópica, o manejo quirúrgico de la ventana lateral se podría utilizar sólo con anestesia local para realizar dicho procedimiento 59]
El factor clave para el éxito de la recuperación de la función del seno maxilar, más allá de la eliminación de un cuerpo extraño a partir del seno maxilar, es la recreación de la permeabilidad adecuada del ostium maxilar.[66]
Esto se puede obtener con cirugía endoscópica, que tiene las siguientes ventajas: procedimiento menos invasivo, posibilidad de control, el tratamiento del antro maxilar, y la ampliación del ostium maxilar obstruido, esto para permitir la recuperación rápida de las funciones del seno maxilar.
Las complicaciones graves vinculadas con la cirugía endoscópica son menos de 0.1% y en general son consecuencia de errores técnicos. El único efecto secundario reportado en la literatura es la formación de sinequias debido a la formación de la cicatriz entre el cornete inferior y el tabique nasal. Esta complicación, que puede ser considerada de relevancia clínica limitada, puede ser una consecuencia del trauma quirúrgico inducido por los instrumentos endoscópicos utilizados durante el procedimiento.[67]
Mareo o vértigo
La aparición de mareo de rotación provocado por movimientos de la cabeza o cambio de postura, es benigno porque no es una condición progresiva y no permanece a lo largo de la vida; es paroxismal porque es repentino y su aparición impredecible; es posicional porque ocurre con ciertos cambios en la posición de la cabeza. Cuando se realiza la EPSN, el trauma quirúrgico, con la técnica de osteótomos, puede causar el desprendimiento de los otolitos, disfunción que es conocida como otoconia de la mácula utricular.[68] El origen de estos mareos puede seguir a una infección viral, trastornos vasculares y trauma en la cabeza. Este mareo es autolimitante y los síntomas disminuyen o desaparecen en el rango de tres a seis meses de su inicio. Se encontraron varios reportes de caso en pacientes sometidos a elevación de seno maxilar con técnica crestal, [69] donde hubo resolución de los síntomas entre cuatro semanas y seis meses. Los casos de cefalea, laberintitis, se han reportado después de la utilización del abordaje crestal propuesto por Summer para la EPSM.
Para buscar asociación entre esta condición y el uso del martillado con los osteótomos, Peñarrocha et al, [68] reportan una prevalencia del 1,25% de los casos que se realizaron con esta técnica. Por otro lado, Sammartino et al, [70] realizaron un ensayo clínico aleatorizado, y muestran que hay una prevalencia relativamente baja pero se debe tener en cuenta con esta técnica de osteótomos la posibilidad de mareos cuando se realiza la EPSM.
REFERENCIAS BIBLIOGRÁFICAS
- Ziccardi VB, Betts NJ. Complications of maxillary sinus augmentation. En: Ziccardi VB. The sinus bone graft. Chicago: Quintessence Publishing; 1999. p. 201-208
- Testori T, Weinstein RL, Taschieri S, Del Fabbro M. Risk factor analysis following maxillary sinus augmentation: a retrospective multicenter study. Int J Oral Maxillofac Implants. 2012; 27(5): 1170-6.
- Sperber GH. Applied anatomy of the maxillary sinus. J Can Dent Assoc. 1980; 46(6): 381-6.
- Chanavaz M. Maxillary sinus: anatomy, physiology, surgery, and bone grafting related to implantology: eleven years of surgical experience (1979-1990). J Oral Implantol. 1990; 16(3): 199-209.
- Briceño JF, Estrada JH. Elevación de piso de seno maxilar: consideraciones anatómicas y clínicas. Revisión de la literatura. Univ Odontol. 2012; 31(67): 27-55.
- Figun ME, Garino RR. Anatomia odontológica funcional y aplicada. 2a Buenos Aires: El Ateneo; 1980.
- Radi JN, Becerra F, Otálvaro N. Cirugía de elevación del piso de seno maxilar. I. Consideraciones básicas generales. Rev Fac Odontol Univ Antioq. 2003; 14(1): 84-91.
- Neugebauer J, Ritter L, Mischkowski RA, Dreiseidler T, Scherer P, Ketterle M, et al. Evaluation of maxillary sinus anatomy by cone-beam CT prior to sinus floor elevation. Int J Oral Maxillofac Implants. 2010; 25(2): 258-65.
- Stover J. The incidence, localization and height of maxillary sinus septa in the edentulous and dentate maxilla. J Oral Maxillofac Surg. 1999; 57(6): 671-2.
- Rodella LF, Buffoli B, Labanca M, Rezzani R. A review of the mandibular and maxillary nerve supplies and their clinical relevance. Arch Oral Biol. 2012; 57(4): 323-34. doi: 10.1016/j.archoralbio.2011.09.007.
- Kantarci M, Karasen RM, Alper F, Onbas O, Okur A, Karaman A. Remarkable anatomic variations in paranasal sinus region and their clinical importance. Eur J Radiol. 2004; 50(3): 296-302.
- Griffa A, Berrone M, Boffano P, Viterbo S, Berrone S. Mucociliary function during maxillary sinus floor elevation. J Craniofac Surg. 2010; 21(5): 1500-2. doi: 10.1097/SCS.0b013e3181ef2be9.
- Boyne PJ, James RA. Grafting of the maxillary sinus floor with autogenous marrow and bone. J Oral Surg. 1980; 38(8): 613-6.
- Chen ST, Beagle J, Jensen SS, Chiapasco M, Darby I. Consensus statements and recommended clinical procedures regarding surgical techniques. Int J Oral Maxillofac Implants. 2009; 24 Suppl: 272-8.
- Aghaloo TL, Moy PK. Which hard tissue augmentation techniques are the most successful in furnishing bony support for implant placement. Int J Oral Maxillofac Implants. 2007; 22 Suppl: 49-70.
- Breinbauer H, Contreras JM, Namoncura C. Técnica de Caldwell-Luc en los últimos 16 años: Revisión de sus indicaciones. Otorrinolaringol. Cir. Cabeza Cuello. 2008; 68(3): 247-54.
- van den Bergh JP, ten Bruggenkate CM, Disch FJ, Tuinzing DB. Anatomical aspects of sinus floor elevations. Clin Oral Implants Res. 2000; 11(3): 256-65.
- Summers RB. Sinus floor elevation with osteotomes. J Esthet Dent. 1998; 10(3): 164-71.
- Summers RB. The osteotome technique: Part 2 – The ridge expansion osteotomy (REO) procedure. Compendium. 1994; 15(4): 422, 424, 426, passim; quiz 436.
- Summers RB. The osteotome technique: Part 3 – Less invasive methods of elevating the sinus floor. Compendium. 1994; 15(6): 698, 700, 702-4 passim; quiz 710.
- Summers RB. The osteotome technique: Part 4 – Future site development. Compend Contin Educ Dent. 1995; 16(11): 1090, 1092 passim; 1094-1096, 1098, quiz 1099.
- Ucer C. Nasal suction technique for maxillary sinus floor elevation: a report of 24 consecutive patients. Int J Oral Maxillofac Implants. 2009; 24(6): 1138-43.
- Chen L, Cha J. An 8-year retrospective study: 1,100 patients receiving 1,557 implants using the minimally invasive hydraulic sinus condensing technique. J Periodontol. 2005; 76(3): 482-91.
- Vitkov L, Gellrich NC, Hannig M. Sinus floor elevation via hydraulic detachment and elevation of the Schneiderian membrane. Clin Oral Implants Res. 2005; 16(5): 615-21.
- Cosci F, Luccioli M. A new sinus lift technique in conjunction with placement of 265 implants: a 6-year retrospective study. Implant Dent. 2000; 9(4): 363-8.
- Chiapasco M, Zaniboni M, Rimondini L. Dental implants placed in grafted maxillary sinuses: a retrospective analysis of clinical outcome according to the initial clinical situation and a proposal of defect classification. Clin Oral Implants Res. 2008; 19(4): 416-28. doi: 10.1111/j.1600-0501.2007.01489.x.
- Uchida Y, Goto M, Katsuki T, Soejima Y. Measurement of maxillary sinus volume using computerized tomographic images. Int J Oral Maxillofac Implants. 1998; 13(6): 811-8.
- Garbacea A, Lozada JL, Church CA, Al-Ardah AJ, Seiberling KA, Naylor WP, et al. The incidence of maxillary sinus membrane perforation during endoscopically assessed crestal sinus floor elevation: a pilot study. J Oral Implantol. 2012; 38(4): 345-59. doi: 10.1563/AAID-JOI-D-12-00083.
- Vlassis JM, Fugazzotto PA. A classification system for sinus membrane perforations during augmentation procedures with options for repair. J Periodontol. 1999; 70(6): 692-9.
- Oh E, Kraut RA. Effect of sinus membrane perforation on dental implant integration: a retrospective study on 128 patients. Implant Dent. 2011; 20(1): 13-9. doi: 10.1097/ID.0b013e3182061a73.
- Robiony M, Tenani G, Sbuelz M, Casadei M. A simple method for repairing membrane sinus perforation. Open Journal of Stomatology. 2012; 2(4): 348-351.
- Hernández F, Torradeflot MM, Marti C. Prevalence and management of Schneiderian membrane perforations during sinus-lift procedures. Clin Oral Implants Res. 2008; 19(1): 91-8. Epub 2007 Oct 23.
- Wallace S. Complications in lateral window sinus elevation surgery. En: Froum SJ, editor. Dental implant complications: Etiology, prevention, and treatment. Oxford: Wiley-Blackwell; 2010. p. 284-309.
- Molly L. Bone density and primary stability in implant therapy. Clin Oral Implants Res. 2006; 17 Suppl 2:124-35.
- Lekholm U, Zarb G. Patient selection and preparation. En: Brånemark P-I, Zarb GA, Albrektsson T. Tissue-integrated prostheses: osseointegration in clinical dentistry. Chicago: Quintessence; 1985. p. 199-209.
- Misch CE. Prótesis dental sobre implantes. Madrid: Elsevier; 2006.
- Misch CE. Implantología contemporánea. Madrid: Mosby- Doyma; 1995.
- Testori T, Rosano G, Taschieri S, Del Fabbro M. Ligation of an unusually large vessel during maxillary sinus floor augmentation. A case report. Eur J Oral Implantol. 2010; 3(3): 255-8.
- Jensen SS, Eriksen J, Schiodt M. Severe bleeding after sinus floor elevation using the transcrestal technique: a case report. Eur J Oral Implantol. 2012; 5(3): 287-91.
- Anavi Y, Allon DM, Avishai G, Calderon S. Complications of maxillary sinus augmentations in a selective series of patients. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2008; 106(1): 34-8.
- Zinner ID, Small SA. Sinus-lift graft: using the maxillary sinuses to support implants. J Am Dent Assoc. 1996; 127(1): 51-7.
- Timmenga NM, Raghoebar GM, Liem RS, van Weissenbruch R, Manson WL, Vissink A. Effects of maxillary sinus floor elevation surgery on maxillary sinus physiology. Eur J Oral Sci. 2003; 111(3): 189-97.
- Regev E, Smith RA, Perrott DH, Pogrel MA. Maxillary sinus complications related to endosseous implants. Int J Oral Maxillofac Implants. 1995; 10(4): 451-61.
- Temmerman A, Hertelé S, Teughels W, Dekeyser C, Jacobs R, Quirynen M. Are panoramic images reliable in planning sinus augmentation procedures? Clin Oral Implants Res. 2011; 22(2): 189-94. doi: 10.1111/j.1600-0501.2010.02000.x. Epub 2010 Sep 27.
- Perella A, Rocha S, Cavalcanti M. Quantitative analyses of maxillary sinus using computed tomography. J Appl Oral Sci. 2003; 11(3): 229-33.
- Greenstein G, Cavallaro J, Romanos G, Tarnow D. Clinical recommendations for avoiding and managing surgical complications associated with implant dentistry: a review. J Periodontol. 2008; 79(8): 1317-29. doi: 10.1902/jop.2008.070067 .
- Park SH, Wang HL. Implant reversible complications: classification and treatments. Implant Dent. 2005; 14(3): 211-20.
- Sadig W, Almas K. Risk factors and management of dehiscent wounds in implant dentistry. Implant Dent. 2004; 13(2): 140-7.
- Drake RL, Wayne A, Mitchell A. Anatomía de Gray para estudiantes. 3a Madrid: Elsevier; 2015. p. 26,42,56,93.
- Barone A, Santini S, Sbordone L, Crespi R, Covani U. A clinical study of the outcomes and complications associated with maxillary sinus augmentation. Int J Oral Maxillofac Implants. 2006; 21(1): 81-5.
- Pjetursson BE, Tan WC, Zwahlen M, Lang NP. A systematic review of the success of sinus floor elevation and survival of implants inserted in combination with sinus floor elevation. Part I: Lateral approach. J Clin Periodontol. 2008; 35 (Suppl. 8): 216–240.
- Laboratorio de antropología física y anatomía humana. Módulo 1: nomenclatura anatómica y generalidades osteoarticular [Internet]. Valparaíso: Pontificia Universidad Católica de Valparaíso, Grupo del laboratorio de antropología física y anatomía humana; [consultado 2016 Jul 03]. Disponible en: http://www.anatomiahumana.ucv.cl/efi/modulo1.html.
- Brook I. Sinusitis. Periodontol 2000. 2009; 49: 126-39. doi: 10.1111/j.1600-0757.2008.00293.x.
- Guía de Práctica Clínica, Diagnóstico y tratamiento de sinusitis aguda, México: Secretaria de Salud; 2009.
- Rosenfeld RM, Piccirillo JF, Chandrasekhar SS, Brook I, Ashok Kumar K, Kramper M. Clinical practice guideline (update): adult sinusitis. Otolaryngol Head Neck Surg. 2015; 152(2 Suppl): S1-S39. doi: 10.1177/0194599815572097.
- Okuyemi KS, Tsue TT. Radiologic imaging in the management of sinusitis. Am Fam Physician. 2002; 66(10): 1882-6.
- Ahovuo A, Borisenko OV, Kovanen N, Varonen H, Rautakorpi UM, et al. Antibiotics for acute maxillary sinusitis. Cochrane Database Syst Rev. 2008; (2): CD000243. doi: 10.1002/14651858.CD000243.pub2.
- Venekamp RP1, Thompson MJ, Hayward G, Heneghan CJ, Del Mar CB, Perera R. Systemic corticosteroids for acute sinusitis. Cochrane Database Syst Rev. 2014; (3): CD008115. doi: 10.1002/14651858.CD008115.pub3.
- Chiapasco M, Felisati G, Maccari A, Borloni R, Gatti F, Di Leo F. The management of complications following displacement of oral implants in the paranasal sinuses: a multicenter clinical report and proposed treatment protocols. Int J Oral Maxillofac Surg. 2009; 38(12): 1273-8. doi: 10.1016/j.ijom.2009.09.001. Epub 2009 Sep 24.
- Stewart MG, Johnson RF. Chronic sinusitis: symptoms versus CT scan findings. Curr Opin Otolaryngol Head Neck Surg. 2004; 12(1): 27-9.
- Jebreel A, Wu K, Loke D, Stafford N. Chronic Rhinosinusitis: Role of CT scans in the evaluation of paranasal sinuses. The Internet Journal of Otorhinolaryngology. 2007; 6(2): 15288420.
- Falk H, Ericson S, Hugoson A. The effects of periodontal treatment on mucous membrane thickening in the maxillary sinus. J Clin Periodontol. 1986; 13(3): 217-22.
- Ramotar H, Jaberoo MC, Koo Ng NK, Pulido MA, Saleh HA. Image-guided, endoscopic removal of migrated titanium dental implants from maxillary sinus: two cases. J Laryngol Otol. 2010; 124(4): 433-6. doi: 10.1017/S0022215109990958. Epub 2009 Sep 1.
- Peleg M, Mazor Z, Chaushu G, Garg AK. Sinus floor augmentation with simultaneous implant placement in the severely atrophic maxilla. J Periodontol. 1998; 69(12): 1397-403.
- Alexander G, Attia H. Oral maxillofacial surgery displacement complications. Oral Maxillofac Surg Clin North Am. 2011; 23(3): 379-86. doi: 10.1016/j.coms.2011.04.001.
- Del Fabbro M, Testori T, Francetti L, Weinstein R. Systematic review of survival rates for implants placed in the grafted maxillary sinus. Int J Periodontics Restorative Dent. 2004; 24(6): 565-77.
- Stammberger H, Posawetz W. Functional endoscopic sinus surgery. Concept, indications and results of the Messerklinger technique. Eur Arch Otorhinolaryngol. 1990; 247(2): 63-76.
- Peñarrocha M, Rambla J, Perez V, Pérez H. Benign paroxysmal vertigo secondary to placement of maxillary implants using the alveolar expansion technique with osteotomes: a study of 4 cases. Int J Oral Maxillofac Implants. 2008; 23(1): 129-32.
- Rosen PS. Complications with the bone-added osteotome sinus floor elevation: Etiology, prevention and treatment. En: Froum SJ, editor. Dental implant complications: Etiology, prevention, and treatment. Oxford: Wiley-Blackwell; 2010. p. 284-309.
- Sammartino G, Mariniello M, Scaravilli MS. Benign paroxysmal positional vertigo following closed sinus floor elevation procedure: mallet osteotomes vs. screwable osteotomes. A triple blind randomized controlled trial. Clin Oral Implants Res. 2011; 22(6): 669-72. doi: 10.1111/j.1600-0501.2010.01998.x. Epub 2010 Nov 3.

